AUTOR: Dr. Juan Fco. Rodríguez Moreno
(Las palabras subrayadas pueden encontrarse en el glosario, al final del documento)
El testículo es un órgano par, de morfología ovoidea, cuyas funciones principales son la producción de los espermatozoides y la síntesis y secreción de las hormonas sexuales masculinas. Los testículos se encuentran en el escroto, una bolsa de piel que los protege. Cada testículo está suspendido de un cordón espermático, el cual contiene los vasos sanguíneos, nervios del propio testículo, y el conducto deferente por el que ascienden los espermatozoides desde el epidídimo.
Los testículos tienen varias tipos de células en su estructura con distintas funciones. De todas ellas la población más relevante para el tema que aquí nos ocupa es la de unas células denominadas células germinales, las cuales por efecto de las hormonas masculinas madurarán para dar lugar a los espermatozoides a partir de la adolescencia. El 90% de los tumores malignos del testiculo se generan a partir de esas células germinales. De ahí que al cáncer de testículo se le denomine también Tumor de Células Germinales (TCG) siendo términos en general equivalentes.
El cáncer de testículo es el tumor más frecuente en hombres entre los 15 y los 35 años. Sin embargo, tras este pico de incidencia se convierte en una rareza y, en general sólo supone el 1% del total de los tumores diagnosticados en varones. En España, se estima que se diagnosticarán 1510 casos en este año 2023. Su frecuencia varia en los diferentes países por motivos que desconocemos.
Desde los años 90 el número de casos diagnosticados va en aumento por causas que se desconocen aunque la mortalidad ha descendido, reflejando las mejoras en el tratamiento de estos pacientes y su diagnóstico cada vez más precoz.
Afortunadamente, la gran mayoría de los pacientes se curan, incluso en aquellos casos en los que la enfermedad se presenta inicialmente ya muy avanzada. Esto es posible fundamentalmente gracias a los esquemas de quimioterapia basados en un fármaco que se llama cisplatino y que se comenzaron a desarrollar durante la década de los 70 del siglo pasado.
Causas y factores de riesgo
La causa concreta del cáncer de testículo resulta desconocida, al igual que la de otros muchos tumores; pero sí se han identificado algunos factores de riesgo con una clara asociación con los tumores germinales.
El principal factor de riesgo es la Criptorquidia (falta de descenso del testículo hasta el escroto durante los primeros años de vida). Durante el desarrollo del embrión, los testículos descienden desde la zona cefálica (lo que después corresponderá a la cabeza) hasta su lugar definitivo en el escroto a través de la línea media y el abdomen. En algunos casos, este descenso no se produce o se retrasa hasta después del nacimiento. Los varones con criptorquidia tienen un mayor riesgo de presentar cáncer tanto en el testículo no descendido como en el otro; y de hecho, las guías clínicas recomiendan extirpar de forma preventiva (orquiectomía profiláctica) aquellos testículos finalmente alojados en el abdomen que no terminan de descender.
Entre el 1 y el 3% de los pacientes con tumores germinales tienen historia familiar de cáncer de testículo, lo cual sugiere un cierto componente hereditario. Además, los hermanos o los hijos de estos enfermos tienen hasta 10 veces más riesgo de desarrollar la enfermedad. Sin embargo todavía no están bien establecidos los factores genéticos responsables. Trabajos recientes llevados a cabo en población española apuntan a que probablemente no exista un gen único o una mutación concreta predisponente sino posiblemente una combinación de diferentes genes alterados.
Prevención y técnicas de diagnóstico precoz
En términos generales no existe ninguna forma de prevenir el cáncer de testículo, porque no se conoce ningún factor de riesgo que se pueda evitar. Además la frecuencia de la enfermedad es baja, incluso en las personas que presentan factores de riesgo. Por otra parte, sí está demostrado que la Orquidopexia (intervención mediante la cual se baja y fija un testículo no descendido al escroto de forma natural) previene el desarrollo de cáncer de testículo en el subgrupo de los niños con criptorquidia.
No está recomendada realización de exploraciones o pruebas rutinarias para diagnosticarlo de forma precoz en la población general, dado que es un tumor poco frecuente, de fácil diagnóstico en estadios iniciales y de buen pronóstico. Sin embargo sí es importante que la población diana de esta enfermedad (varones entre 15-35 años) esté familiarizada con los signos y síntomas de alarma más comunes.
Signos y síntomas al diagnóstico
La gran mayoría de los tumores germinales del varón se diagnostican porque el paciente se palpa un bulto en el testículo, que con frecuencia no duele. En los casos en los que existe dolor, suele aparecer progresivamente, aunque puede hacerlo de forma repentina si el tumor se complica con una infección (orquiepididimitis) o si sangra. En general los pacientes describen más una sensación de peso en el área genital o simplemente un aumento de tamaño del testículo.
En casos mucho más raros, estos tumores pueden ocasionar un crecimiento de las mamas en varones (ginecomastia) por el aumento de la Beta-Gonadotropina Coriónica (β-HCG), una hormona que se produce durante el embarazo y que solo aumenta en varones con ciertos tipos de tumores testiculares. En algunos pacientes puede existir dolor de espalda o de abdomen, causado porque los estímulos dolorosos del testículo se dirigen hacia ese lugar, o bien porque existan metástasis (extensiones del tumor de testículo a otras zonas) en ganglios linfáticos de la parte más posterior del abdomen (retroperitoneo).
Por último, en los casos en los que existen metástasis en otros órganos (por ejemplo en el pulmón, cerebro, hueso, etc.), éstas pueden producir síntomas muy variados (falta de aire, inestabilidad, dolor, etc.), dependiendo de su localización.
Tipos histológicos
Los tipos histológicos son las distintas clases de tumores que se pueden desarrollar en un órgano. Estos tipos vienen determinados en función de las características microscópicas del tumor.
En el caso de los tumores de testículo cuando la célula germinal crece de una forma anómala puede seguir distintos patrones y dar lugar a dos grandes familias de tumores:
- Seminomas: Estos representan aproximadamente el 50% de los tumores germinales. Para que un tumor de testículo se considere seminoma, no debe estar mezclado con otros tipos de tumor. Existen dos subtipos:
o Seminoma Clásico
o Seminoma Atípico
- No seminomas: Cuando hablamos de “no seminoma” en realidad hacemos alusión a un grupo que incluye a varios posibles subtipos:
* Carcinoma embrionario
* Coriocarcinoma
* Tumor del seno endodérmico
* Teratoma
El subtipo mas frecuente es el carcinoma embrionario, si bien los pacientes suelen tener tumores mixtos que mezclan en distinta proporción cualquiera de estos subtipos e incluso partes de seminoma (en este caso particular, se continúan considerando no seminmas).
Estudios diagnósticos
Cuando se aborda un probable caso de cáncer de testículo, además de preguntar por los síntomas y explorar al paciente, se completa el estudio con las siguientes pruebas complementarias:
- Analítica general, incluyendo LDH, alfa-fetoproteína y β-hCG. Estas sustancias se utilizan en el caso de los tumores germinales como marcadores tumorales. Son proteínas producidas por las células del tumor y van a resultar muy útiles para el diagnóstico y/o el seguimiento de la enfermedad. La β-HCG puede estar elevada en cualquier tipo de tumor de testículo, mientras que la alfa-fetoproteína solo aumenta en los tumores no seminomatosos. La LDH (lactatodeshidrogenasa) es otra proteína presente en la sangre que también se eleva en algunos pacientes con tumores de testículo, y deberá vigilarse su evolución durante el tratamiento. Sin embargo, como ocurre en otros tipos de cáncer, los marcadores tumorales no aumentan en todos los pacientes con cáncer de testículo; ni tampoco cualquier elevación de estas proteínas se corresponde inequívocamente con el hecho de tener un tumor germinal.
- Ecografía del testículo: Es una prueba crucial, ya que nos permite distinguir un tumor de otras entidades benignas que también podrían ocasionar un nódulo palpable en el testículo. Si definitivamente se confirma la existencia de una tumoración, mediante ecografía se pueden observar las características de la misma (localización, tamaño, vascularización, etc.), explorar el testículo contralateral, etc.
- Tomografía axial computerizada (TAC) del tórax, abdomen y pelvis: Permiten estudiar el resto de órganos del cuerpo y las principales vías de drenaje linfático testicular, de manera que es imprescindible para una correcta estadificación del caso.
Además pueden realizarse en algunos casos:
- TAC o resonancia nuclear magnética (RNM) cerebral: si se sospecha la existencia de metástasis cerebrales
- Gammagrafía ósea: si se sospecha la existencia de metástasis óseas.
-
Tomografía por Emisión de Positrones (
PET): se utiliza en ocasiones para valorar los restos de tumor que pueden persistir tras el tratamiento quimioterápico inicial en casos de enfermedad avanzada (ver sección de
tratamiento). El PET no esta indicado como procedimiento de rutina en el diagnostico inicial de todos los casos.
Estadios
En general todos los tumores se clasifican en varios estadios (en función de parámetros como su tamaño, órganos afectos, diseminación a distancia, etc.) que tendrán una evolución diferente y requerirán tratamientos distintos. En el caso del cáncer de testículo la clasificación más empleada es el sistema TNM, que valora la extensión del propio tumor primario (T, tumor primario), la afectación de ganglios linfáticos (N, del inglés “nodes” o ganglios), la presencia de metástasis a distancia (M) y el grado de elevación de los marcadores tumorales en la sangre (S, del inglés serum o suero). De forma simplificada, la clasificación presenta los siguientes estadios:
- Estadio I: el tumor sólo afecta al testículo.
- Estadio II: el tumor se extiende a ganglios linfáticos, normalmente localizados en el retroperitoneo (la zona que se encuentra en la parte posterior del abdomen).
- Estadio III: el tumor presenta metástasis o elevación muy importante de los marcadores tumorales.
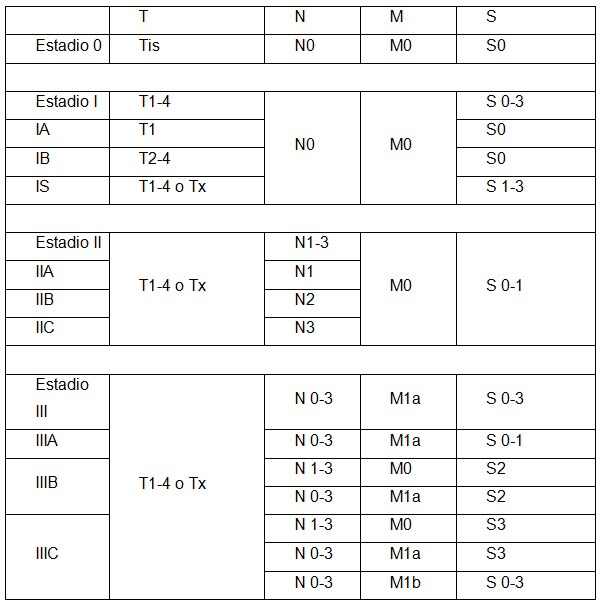
A continuación se presenta el sistema completo de clasificación por estadios de los tumores de testículo. Se emplea asignando a cada caso una clasificación en función de las características del tumor primario (T, tabla 1), de los ganglios linfáticos (N, tabla 2), de la presencia o no de metástasis (M, tabla 3) y de la elevación de los marcadores tumorales (S, tabla 4). Con estos cuatro factores, cada tumor se clasifica por estadios según los criterios expresados en la última tabla (agrupación por estadios, tabla 5):
- Tabla 1: tumor primario (T)
|
TX
|
No puede evaluarse el tumor primario: normalmente porque no se ha realizado la extirpación quirúrgica del testículo (orquiectomía)
|
|
T0
|
No se encuentra el tumor primario: puede ocurrir si el tumor desaparece de forma espontánea, o también si el tumor se ha originado en un lugar distinto del testículo (ver factores pronósticos)
|
|
Tis
|
Neoplasia celular intratubular (carcinoma in situ): es un tumor no invasivo
|
|
T1
|
Tumor limitado al testículo que no invade los vasos sanguíneos o linfáticos; el tumor puede invadir la túnica albugínea pero no la túnica vaginal (distintas capas o cubiertas del testículo)
|
|
T2
|
Tumor limitado al testículo y epidídimo que invade los vasos sanguíneos o linfáticos; o tumor que se extiende a través de la túnica albugínea afectando a la túnica vaginal (distintas capas o cubiertas del testículo)
|
|
T3
|
Tumor que invade el cordón espermático con o sin invasión de los vasos sanguíneos o linfáticos.
|
|
T4
|
Tumor que invade el escroto con o sin invasión de los vasos sanguíneos o linfáticos.
|
Estas clasificaciones se realizan tras analizar el tumor después de la intervención quirúrgica.
- Tabla 2: ganglios linfáticos (N)
|
NX
|
No pueden evaluarse los ganglios linfáticos.
|
|
N0
|
No hay metástasis en ganglios linfáticos
|
|
N1
|
Metástasis en un solo ganglio linfático menor de 2 cm. O en varios ganglios linfáticos, ninguno mayor de 2 cm.
|
|
N2
|
Metástasis en un solo ganglio linfático con diámetro entre 2-5 cm.; o ganglios linfáticos múltiples con diámetro mayor de 2-5 cm.
|
|
N3
|
Metástasis en ganglios linfáticos con diámetro mayor de 5 cm.
|
- Tabla 3: Metástasis a distancia (M)
|
MX
|
No puede evaluarse la presencia de metástasis a distancia
|
|
M0
|
No hay metástasis a distancia
|
|
M1
|
Existen metástasis a distancia
|
|
M1a
|
Metástasis pulmonares o en ganglios lejanos al testículo
|
|
M1b
|
Metástasis a distancia en zonas distintas a los pulmones y ganglios lejanos al testículo
|
- Tabla 4: Marcadores tumorales séricos (S)
|
Sx
|
Marcadores no realizados o no disponibles
|
|
S0
|
Marcadores normales
|
|
S1
|
LDH <1,5 x límite superior de la normalidad; y
β-hCG <5000 mUI/mL; y
AFP <1000 ng/mL
|
|
S2
|
LDH 1,5-10 x límite superior de la normalidad; o
β-hCG 5000-50.000 mUI/mL; o
AFP 1000-10.000 ng/mL
|
|
S3
|
LDH > 10 x límite superior de la normalidad; o
β-hCG >50.000 mUI/mL; o
AFP >10.000 ng/mL
|
AFP: alfa-fetoproteína; β-hCG: beta-gonadotropina coriónica; LDH: lactatodeshidrogenasa.
- Tabla 5: Agrupación por estadios
Factores pronósticos
Los factores pronósticos son características del tumor y del paciente que permiten estimar a priori su evolución posterior, complementando el estadio marcado por el sistema TNM.
En el cáncer de testículo con metástasis tratado con quimioterapia existen 3 factores pronósticos de gran importancia con los que en el año 1997 se elaboró una clasificación pronóstica de enorme alcance, aun vigente, y crítica a la hora de determinar el tratamiento más adecuado para cada enfermo: La Clasificación Pronóstica del International Germ Cell Cancer Collaborative Group (IGCCCG).
Esta clasificación establece 3 categorías para los tumores no seminomatosos (pronóstico favorable, intermedio o desfavorable); y 2 para los seminomatosos (pronóstico favorable o intermedio; no existen pacientes con pronóstico desfavorable en este subtipo histológico). Los factores pronósticos son:
- Que el tumor se origine en el propio testículo (signo de buen pronóstico) o fuera de él. Un pequeño porcentaje de tumores de células germinales pueden presentarse en zonas del cuerpo distintas del testículo, sin que se encuentre tumor en el propio testículo; bien porque el tumor inicial ha desaparecido o porque realmente la enfermedad se originó fuera del testículo. Esto último puede suceder porque durante el desarrollo del embrión el testículo migra hasta su posición final en el escroto. En este trayecto pueden quedar restos de células del testículo que muy raramente ya en la edad adulta pueden dar lugar a tumores.
- La ausencia de metástasis a distancia (M1)(signo de buen pronóstico), con excepción de las metástasis de pulmón que por sí solas no indican mal pronóstico.
- El grado de elevación de los marcadores tumorales. En general, cuanto más elevados, el pronóstico es peor, de acuerdo a los límites señalados en la tabla 6.
A continuación se presenta de forma completa el sistema de clasificación pronóstica del cáncer de testículo con metástasis para los tumores no seminomatosos (tabla 6) y para los seminomatosos (tabla 7). Se incluye la frecuencia de cada grupo, la proporción de pacientes que sobreviven a los 5 años (supervivencia global) y la proporción de pacientes que a los 5 años viven y además no presentan enfermedad (supervivencia libre de progresión).
-
Tabla 6: categorías pronósticas para los tumores no seminomatosos

AFP: alfa-fetoproteína; β-hCG: beta-gonadotropina coriónica; LDH: lactatodeshidrogenasa. LSN: límite superior de la normalidad.
- Tabla 7: categorías pronósticas para los seminomas

Tratamiento
Si bien los tumores germinales del testículo tienen muy buen pronóstico en manos experimentadas, hablamos de neoplasias de muy rápido crecimiento, que suponen una agresión muy importante para el organismo, y que suelen afectar a pacientes muy jóvenes. Es por ello que la principal recomendación internacional es que estos enfermos sean derivados rápidamente a centros especializados con profesionales habituados a su manejo.
Hay que tener en cuenta que, una vez curados, estos pacientes se habrán visto sometidos a tratamientos que merman su capacidad reproductiva, y que impactan en su esfera sexual y de la autoimagen, por lo que debemos prever estos detalles desde el principio, implicar a sus parejas si las hay, preservar esperma si procede, y aconsejar adecuadamente en el momento oportuno.
El tratamiento de los tumores de testículo requiere en primer lugar quitar el testículo mediante una intervención quirúrgica llamada orquiectomía. Éste es uno de los pocos tumores en los que, incluso si la enfermedad se ha extendido a otros órganos se debe quitar el tumor original. Las razones son que los tratamientos de quimioterapia llegan mal al testículo y que el examen del tumor es muy importante para determinar sus características y su tratamiento. La cirugía para quitar el testículo siempre debe realizarse a través de la ingle (vía inguinal) y no a través de la piel del escroto (vía transescrotal), ya que de lo contrario aumentan las posibilidades de contaminación del tejido sano por células del tumor.
Una vez extirpado el testículo, el tratamiento se decide en función:
o Del tipo de tumor (no seminoma o seminoma): el tratamiento de los seminomas y de los tumores no seminomatosos en estadios I y II es distinto, pero en los estadios III es relativamente similar;
o De su extensión (estadio I, II o III); y
o De su categoría pronóstica (favorable, intermedia, o desfavorable).
Aunque aquí se comentan brevemente los tratamientos más habituales, su médico puede proponerle participar en un ensayo clínico como tratamiento de su enfermedad, en cualquier fase de la misma. Los ensayos clínicos prueban nuevos fármacos o técnicas que se cree que pueden mejorar la evolución de la enfermedad. Son diseñados por personas con mucha experiencia en el tratamiento de las enfermedades en las que se realizan los estudios. La participación en un ensayo siempre es voluntaria. Cada ensayo está diseñado para pacientes con unas características determinadas. Su médico le puede informar sobre la posibilidad de participar en un ensayo clínico, así como de sus posibles beneficios e inconvenientes.
Tratamiento de acuerdo a los diferentes estadios
- Estadio I:
Los pacientes con tumores de testículo en estadio I se curan con el tratamiento adecuado en casi el 100% de los casos. Como se ha comentado previamente, estos tumores solo afectan al testículo, por lo que en teoría su extirpación debería ser curativa por sí misma. El problema es que en un pequeño porcentaje de los pacientes la enfermedad puede volver a aparecer. Para evitarlo, en algunos casos se puede administrar tratamiento complementario con intención preventiva (tratamiento adyuvante) que disminuye de forma muy importante el riesgo de que la enfermedad reaparezca. Los tratamientos adyuvantes (tanto quimioterapia como radioterapia) implican riesgos y pueden generar secuelas. Por ejemplo, se sabe que el uso de radioterapia adyuvante en pacientes jóvenes favorece la aparición de leucemias o segundos tumores como cáncer digestivo o de vejiga pasados entre 20 y hasta 40 años del tratamiento inicial. Con el uso de quimioterapia se tiene menos experiencia pero sí se ha comprobado que la administración de quimioterapia en la juventud aumenta el riesgo cardiovascular pasados los años. Por tanto hay que evitar el sobretratamiento e intentar seleccionar solo a los pacientes que verdaderamente presentan un riesgo de reaparición de la enfermedad. Incluso algunas corrientes aconsejan no tratar de forma preventiva a nadie y sólo administrar quimioterapia a los enfermos que recaigan ya que, incluso en esos casos, la enfermedad suele ser controlable y las opciones de curación muy altas.
o Seminoma:
El 80% de los pacientes quedan curados tras la orquiectomía, pero en un 20% de los casos, la enfermedad puede volver a aparecer. Por lo tanto, en los pacientes con seminoma estadio I, las alternativas son:
- Administrar quimioterapia con 1 ó 2 ciclos de un fármaco llamado carboplatino. Este tratamiento es bien tolerado y disminuye el riesgo de recaida a un 3-4%.
- No administrar ningún tratamiento y realizar observación cuidadosa del paciente (ver sección de seguimiento). Así se evita realizar tratamientos innecesarios a pacientes que realmente no iban a tener una recaída.
- Tratamiento con radioterapia retroperitoneal. Estos tumores son muy radiosensibles y la radioterapia es eficaz para tratarlos. Sin embargo hoy en día esta opción terapéutica es menos empleada por las toxicidades tardías ya comentadas anteriormente.
Hoy en día, en nuestro medio, el tratamiento más empleado es la quimioterapia o la realización de observación. Dado que hasta el 80% de los pacientes no necesitan quimioterapia, porque están curados con la cirugía, se han intentado identificar factores de riesgo para ayudar a decidir que pacientes deben recibir quimioterapia y cuales deben ser vigilados. Aunque esta estrategia se emplea de forma habitual en muchos centros con buenos resultados, su uso no es universal. Los criterios de riesgo para que la probabilidad de que la enfermedad reaparezca sea mayor son que el tumor mida más de 4 cm. y/o que invada una estructura denominada la rete testis o red testicular (una pequeña red de conductos por los que el semen sale del testículo). Sin embargo la capacidad predictiva de estos factores es inclusive limitada por lo que no se puede universalizar una estrategia basada en el riesgo.
En caso de que la enfermedad reaparezca, tanto si se ha administrado tratamiento complementario como si no, el tratamiento debe adecuarse al caso de un tumor avanzado (ver sección de tratamiento de estadios II y III). En estos casos, el pronóstico suele también ser bueno, pero el tratamiento es más complejo e intenso.
o No seminoma:
En los tumores no seminomatosos aproximadamente el 75% de los pacientes se curan solamente con cirugía, pero en el resto la enfermedad puede volver a aparecer. Hoy en día no disponemos de factores que nos segreguen bien que pacientes van a recaer y cuales no.
En principio, aquellos pacientes cuyo tumor invade los vasos sanguíneos o los vasos linfáticos del testículo tienen más riesgo de que la enfermedad reaparezca. En este caso podría estar mas justificado tratar de forma preventiva con quimioterapia mediante la administración de dos ciclos con unos fármacos llamados bleomicina, etopósido y cisplatino (BEP). Sin embargo con esta estrategia estaríamos sobretratando a un porcentaje de pacientes próximo al 50% que nunca van a recaer tras ser operados.
Los pacientes cuyo tumor no invade los vasos sanguíneos o linfáticos, tienen menos riesgo de que la enfermedad reaparezca y en ellos se tiende a ser menos agresivo y en términos generales se tiende a hacer únicamente un seguimiento cuidadoso (ver sección de
seguimiento).
Otra opción es vigilar a todos los pacientes y no tratar más que a aquellos en los que la enfermedad reaparezca para evitar realizar tratamientos innecesarios, como ya comentamos anteriormente.
También en los tumores no seminomatosos, en caso de que la enfermedad reaparezca, tanto si se ha administrado quimioterapia complementaria como si no, el tratamiento se adecua al escenario de tumor avanzado (ver sección de
tratamiento de estadios II y III).
- Estadio II:
Los pacientes con estadio II tienen enfermedad en los ganglios del retroperitoneo (ver sección de Estadios). La mayoría de estos pacientes también se curan con un tratamiento adecuado.
o Seminoma: el tratamiento habitual de estos pacientes consiste en quimioterapia con 3 ciclos de BEP o cuatro ciclos de cisplatino y etopósido (EP), que consiguen un resultado equivalente.
En algunos pacientes, después de estos tratamientos quedan restos de los ganglios linfáticos del retroperitoneo que no desaparecen por completo. Ante esta situación hay dos opciones en función del tamaño de la masa residual (restos del tumor).
En aquellas masas residuales mayores de 3 cm se debe plantear la realización de un PET para confirmar o desmentir si hay enfermedad viable o es solo necrosis (Celulas muertas) o fibrosis. En lesiones residuales menores de 3 cm no es preciso ninguna intervención y basta con seguir al paciente de forma rutinaria.
o No seminoma: en estos pacientes, el tratamiento más habitual es administrar quimioterapia con 3 ciclos de BEP.
También en estos pacientes pueden quedar restos de los ganglios linfáticos del retroperitoneo que no desaparecen por completo.
En estos casos, cualquier lesión residual > 1 cm debe ser resecada y analizada. El PET NO debe usarse en este contexto salvo situaciones muy excepcionales.
- Estadio III:
En estos pacientes el tratamiento se realiza de forma similar tanto en tumores no seminomatosos como en seminomas. Estos pacientes se deben clasificar de acuerdo a los criterios de riesgo que presenten (ver factores pronósticos) y tratar según el grupo de riesgo al que pertenezcan.
o Pacientes con pronóstico favorable: el tratamiento consiste en 3 ciclos de BEP o 4 de EP.
o Pacientes con pronóstico intermedio o desfavorable: el tratamiento consiste en 4 ciclos de BEP. En algunos pacientes se ofrecen otras alternativas, como esquemas de quimioterapia distintos o quimioterapia a dosis altas con soporte de progenitores de médula ósea, ocasionalmente en el contexto de ensayos clínicos, con el objetivo de intentar mejorar los resultados del tratamiento.
- Fracasos del tratamiento o recaídas:
En los pacientes en los que el tumor no responde al tratamiento o cuando a pesar de responder inicialmente, vuelve a aparecer, lo más frecuente es administrar otras quimioterapias distintas de la inicial. Las quimioterapias de rescate más utilizadas se conocen por sus siglas: VIP (vinblastina, ifosfamida y cisplatino) o TIP (paclitaxel, ifosfamida y cisplatino). En los pacientes que responden adecuadamente al tratamiento, con frecuencia se valora la posibilidad de administrar tratamiento con dosis muy altas de quimioterapia, extrayendo previamente del paciente las células madre de la médula ósea (que son las que generan las demás células de la sangre) y administrándoselas después, para facilitar su recuperación.
En un pequeño número de pacientes, la enfermedad puede reaparecer de forma localizada en un punto bastante tiempo después del diagnóstico (habitualmente 2 o más años). En estos pacientes, el tratamiento suele consistir en extirpar la enfermedad mediante una intervención quirúrgica, aunque también se puede añadir quimioterapia complementaria.
Si a pesar de todos estos tratamientos la enfermedad no queda curada y vuelve a aparecer, se suelen administrar otros tipos de quimioterapia, o volver a utilizar alguno de los fármacos empleados previamente. Sin embargo en estas situaciones lo habitual es que estos tratamientos solo retrasen el curso de la enfermedad y es poco frecuente que se consiga la curación. En casos seleccionados de refractariedad al tratamiento médico se pueden emplear Cirugías de Rescate, pero todos estos últimos supuestos deben ser planteados únicamente en el contexto de centros de referencia, con posibilidad de incluir a los pacientes en ensayos clínicos y experiencia suficiente.
- Toxicidad del tratamiento de quimioterapia:
Los tratamientos de quimioterapia de combinación empleados en el tratamiento del cáncer de testículo son muy eficaces, pero también son algo más tóxicos que otros tipos de quimioterapia, porque las dosis de los fármacos empleadas son relativamente altas. Además de la toxicidad habitual de la quimioterapia (ver capítulo de efectos secundarios de la quimioterapia), conviene destacar los siguientes puntos:
o Riesgo de infecciones: es bastante habitual que el número de neutrófilos, (los glóbulos blancos que nos protegen frente a las infecciones por bacterias) disminuya de manera relevante. En esta situación es más frecuente que el paciente sufra infecciones y que dichas infecciones sean graves, por lo que en caso de presentar fiebre de más de 38ºC, el paciente debe acudir al servicio médico que le atienda de forma preferente. Su médico puede decidir aplicarle un tratamiento para intentar prevenir que el número de glóbulos blancos descienda.
o Esterilidad: muchos tratamientos de quimioterapia pueden provocar esterilidad inicialmente, habitualmente reversible con el paso del tiempo. Con los tratamientos empleados en el cáncer de testículo, la esterilidad aparece con mucha frecuencia, lo cual es especialmente importante dada la juventud de estos pacientes. Su médico le informará de las alternativas para evitar las consecuencias de la esterilidad.
o Toxicidad pulmonar: la bleomicina empleada en el esquema BEP puede raramente ocasionar fibrosis pulmonar, que consiste en la formación de cicatrices en el pulmón que pueden empeorar su funcionamiento. Si lo considera necesario, su médico puede indicarle que se realice unas pruebas de función respiratoria, antes, durante o después del tratamiento.
Seguimiento
Después del tratamiento del cáncer de testículo es muy importante realizar revisiones periódicas. Las revisiones son más intensas en los pacientes con estadio I en los que se no se administra tratamiento complementario después de la cirugía, porque su riesgo de recurrencia es mayor. En estos pacientes, es frecuente que se realicen controles cada 2 meses, o incluso cada mes, durante el primer y segundo año del diagnóstico.
En las revisiones, además de preguntar por los síntomas y de llevar a cabo una exploración física, suele realizarse una determinación de los marcadores tumorales de los tumores de testículo. Además de forma periódica suele realizarse radiografía de tórax, TAC abdominal y una ecografía de testículo. Según la extensión de la enfermedad al diagnóstico y los síntomas que presente el paciente se pueden añadir otras pruebas distintas.
La frecuencia de las revisiones suele ser variable y su duración es aun tema de debate.
La realidad es que el mayor riesgo de que la enfermedad reaparezca se da en los primeros 2 años tras el diagnostico. Transcurridos los 5 años [que hoy en día se consideran un punto de referencia muy común en oncología] parece lógico referir al paciente a su medico de familia para control anual solo con exploración física y analítica. Otros investigadores estiman que se deberían seguir hasta 10 años y algunos grupos los siguen de por vida.
Glosario
o Alfa-fetoproteína: una proteína producida en el feto que se utiliza como marcador tumoral en algunas enfermedades. Su elevación puede indicar la presencia de un cáncer de testículo de tipo no seminoma, aunque también aumenta en pacientes con cáncer de hígado, hepatitis y en algunos individuos que no presentan tumores.
o BEP: un tratamiento de quimioterapia que contiene unos fármacos llamados bleomicina, etopósido y cisplatino. Se suelen administrar entre 2 y 4 ciclos, según la extensión de la enfermedad. El tratamiento se administra a lo largo de 5 días, más una dosis de bleomicina cada semana. Los ciclos se repiten cada 3 semanas. Es una quimioterapia relativamente agresiva, que se puede administrar estando el paciente ingresado o bien en un hospital de día.
o Beta-gonadotropina coriónica humana (ß-hCG): una hormona que se eleva durante el embarazo. En varones, se eleva únicamente cuando existe un cáncer de testículo, por lo que se emplea como marcador tumoral.
o Biopsia: muestra de tejido que se estudia mediante microscopio y otras técnicas especiales para diagnosticar una enfermedad.
o Carcinoma in situ: un tumor que no es invasivo, superficial.
o Ciclo: cada tanda de quimioterapia. Su duración es variable, pero con mucha frecuencia duran 3 ó 4 semanas, pasadas las cuales el ciclo se repite hasta llegar al número previsto de ciclos (variable en distintas enfermedades, con frecuencia oscila entre 2 y 6 ciclos).
o Cordón espermático: estructura de la cual está suspendido el testículo y que contiene el conducto deferente (un pequeño tubo por donde salen los espermatozoides) y los vasos y nervios del testículo.
o Criptorquidia: falta de descenso del testículo en el momento del nacimiento. Durante el desarrollo del embrión, los testículos descienden desde el abdomen hasta el escroto. En algunos niños, este descenso no se produce u ocurre con retraso después del nacimiento. Es un factor de riesgo para tener un cáncer de testículo.
o Ecografía: prueba de imagen que consiste en utilizar ultrasonidos para valorar distintos órganos.
o Ensayos clínicos: estudios que se realizan en pacientes para desarrollar nuevos tratamientos con la intención de mejorar los resultados. Los ensayos clínicos son diseñados por personas con mucha experiencia en el tratamiento de las enfermedades en las que se realizan los estudios. Son revisados por otros colegas y deben ser valorados y aprobados por Comités Éticos y por el Ministerio de Sanidad, para garantizar la seguridad del paciente. La participación en un ensayo, siempre es voluntaria. Cada ensayo está diseñado para pacientes con unas características determinadas. La Red de Centros Integrales de Cáncer de EE.UU. considera que la mejor opción para cualquier paciente con cáncer es participar en un ensayo clínico. Su médico le puede informar sobre la posibilidad de participar en un ensayo clínico, así como de sus posibles beneficios e inconvenientes.
o EP: una quimioterapia similar al BEP, pero sin bleomicina. Se suele emplear cuando hay alguna contraindicación para administrar bleomicina, habitualmente por alteraciones en la función del pulmón.
o Escroto: bolsa de piel que recubre a los testículos y los protege.
o Gammagrafía ósea: prueba de imagen que consiste en inyectar una sustancia por vía intravenosa que permite valorar si existen metástasis en los huesos, observando como dicha sustancia se deposita en ellos.
o Ganglio linfático: nódulos de tejido linfático que se sitúan en el trayecto de los vasos linfáticos. Por los vasos y por los ganglios circula el líquido linfático que contiene leucocitos y linfocitos, células del sistema inmunológico. Cuando existen en el cuerpo células tumorales o infecciones, están son retenidas en los ganglios linfáticos, por lo que pueden aumentar de tamaño.
o Lactatodeshidrogenasa (LDH): una enzima, es decir una proteína que facilita reacciones químicas en el organismo. Se utiliza como marcador tumoral en algunas enfermedades. Suele aumentar cuando existe destrucción de células y puede indicar muchos trastornos, además del cáncer de testículo.
o Marcador tumoral: una sustancia producida por un tumor que se utiliza para ayudar a realizar su diagnostico y para ver el efecto del tratamiento. En algunos tumores son muy útiles, mientras que en otros muchos no lo son, por lo que en estos casos no se utilizan.
o Mediastino: región del cuerpo que se sitúa entre ambos pulmones, en el tórax.
o Metástasis: extensiones de un tumor a un lugar del cuerpo diferente del sitio de origen (tumor primario). Su presencia indica que el tumor está en un estadio más avanzado.
o Orquiectomía: extirpación quirúrgica del testículo. Se realiza por la ingle (vía inguinal), porque si se realiza a través del escroto, existe riesgo de contaminación del tejido sano por células del tumor.
o PET: tomografía por emisión de positrones. Prueba de imagen que consiste en determinar la captación de glucosa por distintos órganos para valorarlos. Antes de realizar la prueba se administra glucosa marcada de forma especial por vía intravenosa, para facilitar la visión de los diferentes órganos
o RNM: resonancia nuclear magnética. Prueba de imagen que consiste en utilizar las propiedades magnéticas de los distintos tejidos para valorarlos. Antes de realizar la prueba se suele administrar una sustancia llamada contraste por vía intravenosa, para facilitar la visión de los diferentes órganos.
o Retroperitoneo: la zona del cuerpo que está detrás de la cavidad abdominal. Contiene, entre otras estructuras, el páncreas, los riñones y grandes arterias y venas.
o TAC: tomografía axial computerizada. Prueba de imagen que consiste en utilizar radiación para obtener la imagen de distintos órganos y valorarlos. Antes de realizar la prueba se suele administrar una sustancia llamada contraste por vía oral y/ o intravenosa, para facilitar la visión de los diferentes órganos.
o TIP: un tratamiento de quimioterapia que contiene unos fármacos llamados paclitaxel, ifosfamida y cisplatino. Se suele administrar en pacientes en los que el tratamiento inicial no ha funcionado.
o Tratamiento adyuvante: el que se realiza después de una intervención quirúrgica para prevenir la reaparición de la enfermedad. Los pacientes en los que se realizan estos tratamientos no tienen enfermedad visible mediante pruebas diagnósticas, pero pueden tenerla a nivel microscópico.
o VIP: un tratamiento de quimioterapia que contiene unos fármacos llamados vinblastina, ifosfamida y cisplatino. Se suele administrar en pacientes en los que el tratamiento inicial no ha funcionado.